FDA首次批准 Blinatumomab治療特定白血病,有望徹底消除病根
編輯:全球華人抗癌新藥網 來源:全球華人抗癌新藥網 發佈時間:2018-04-02
近日,美國FDA宣佈加速批准安進公司藥物Blincyto(blinatumomab)的擴大適應症申請,用於治療B細胞前體急性淋巴性白血病(ALL),且在緩解期依舊有微小殘留病灶(MRD)的兒童和成人患者。值得一提的是,這是FDA批准的首款治療MRD陽性ALL的療法。
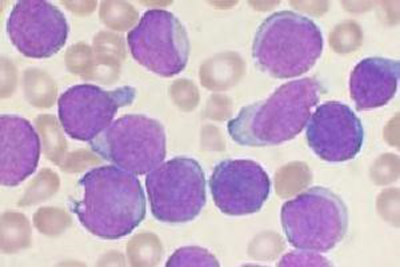
B 細胞前體 ALL 起源於造血系統 B 淋巴母細胞,是克隆性異常增殖所致的惡性疾病,進展快速。患者的骨髓裡會產生過多的不成熟白細胞,影響骨髓的功能,現多採用化療藥物、造血幹細胞移植等治療。經過治療後,依舊會有不少人體內會帶有微小殘留病灶。儘管這些病灶在顯微鏡鏡檢下也無法被發現,但卻給患者留下了疾病復發的隱患。Blinatumomab 主要是通過調節自身免疫功能抵禦這一疾病。
在一項單臂臨床研究裡,Blincyto在MRD陽性ALL的患者中展現出了很好的療效。這些患者曾有1到2次完全緩解,但骨髓裡依然存有癌細胞,比例約占細胞總數的千分之一。在經過治療後,即便是能從10000個細胞裡挑出1個細胞的高精度檢測,也無法在患者體內檢測出MRD,證實了Blincyto的效果。總體來看,有70%的患者再也檢測不出MRD,超過一半的患者已在病情緩解中活過了22.3個月。基於這款新藥的潛力,美國FDA曾授予其孤兒藥資格和優先審評資格。在良好臨床結果下,美國FDA又決定加速批准這款新藥上市,讓它儘快造福患者。
linatumomab 是一種基於雙特異性 T 細胞銜接系統(bispecific T cell engager, BiTE)開發而來的免疫療法。簡單說,它利用一種抗體可以重新定向 T 細胞以毀滅腫瘤細胞。這種療法能夠通過將腫瘤細胞上的 CD19 蛋白(B 細胞衍生的 ALLs 或非霍奇金淋巴瘤表面表達的蛋白質)—一種腫瘤細胞通用抗原呈遞給 CD3 蛋白,進而啟動免疫系統識別和殺滅腫瘤細胞(CD3 是免疫系統中 T 細胞特異表達)。
Blinatumomab 治療相關的常見副作用為發熱、頭痛、周圍性水腫、發熱性中性粒細胞減少、噁心、低鉀血症、乏力、便秘、腹瀉、震顫。需要患者和臨床醫師注意的是,一些臨床試驗患者治療初期,因腫瘤細胞溶解綜合征而出現低血壓和呼吸困難症狀,同樣也有腦病及其它副作用影響中樞神經系統的現象。
帶有MRD的患者更有可能出現復發,因此一種能消除極低量殘餘白血病細胞的療法,有望能幫助延長癌症的緩解期的藥物極為必要。依照計畫,獲得加速批准的Blincyto,依舊需要進行隨機對照試驗,驗證MRD的減少能帶來生存期或無進展生存期的改善。我們期待接下來的試驗同樣能夠順利,患者也能迎來更多控制病情的方法。
